 AmMax Bio evaluiert derzeit AMB-05X, einen selektiven monoklonalen Antikörper, der auf den koloniestimulierenden Faktor-1-Rezeptor (CSF1R) zur Behandlung von tenosynovialen Riesenzelltumoren (TGCT) abzielt. AMB-05X ist speziell für die Verabreichung über verschiedene Verabreichungswege formuliert. Derzeit laufen zwei Phase-2-Studien zum Nachweis des Konzepts - eine Studie zur Bewertung von AMB-05X als lokale, intraartikuläre Injektion in das betroffene Gelenk und eine Studie zur Bewertung von AMB-05X als intravenöse Infusion.
AmMax Bio evaluiert derzeit AMB-05X, einen selektiven monoklonalen Antikörper, der auf den koloniestimulierenden Faktor-1-Rezeptor (CSF1R) zur Behandlung von tenosynovialen Riesenzelltumoren (TGCT) abzielt. AMB-05X ist speziell für die Verabreichung über verschiedene Verabreichungswege formuliert. Derzeit laufen zwei Phase-2-Studien zum Nachweis des Konzepts - eine Studie zur Bewertung von AMB-05X als lokale, intraartikuläre Injektion in das betroffene Gelenk und eine Studie zur Bewertung von AMB-05X als intravenöse Infusion.
Die vorliegende Studie trägt den Titel: Eine adaptive, offene Phase-2-Studie mit ansteigender Mehrfachdosierung zur Bewertung der Wirksamkeit, Sicherheit, Verträglichkeit und Pharmakokinetik von intravenös verabreichtem AMB-05X bei Studienteilnehmer*innen mit tenosynovialem Riesenzelltumor.
Eine schematische Darstellung des Studiendesigns ist unten abgebildet:
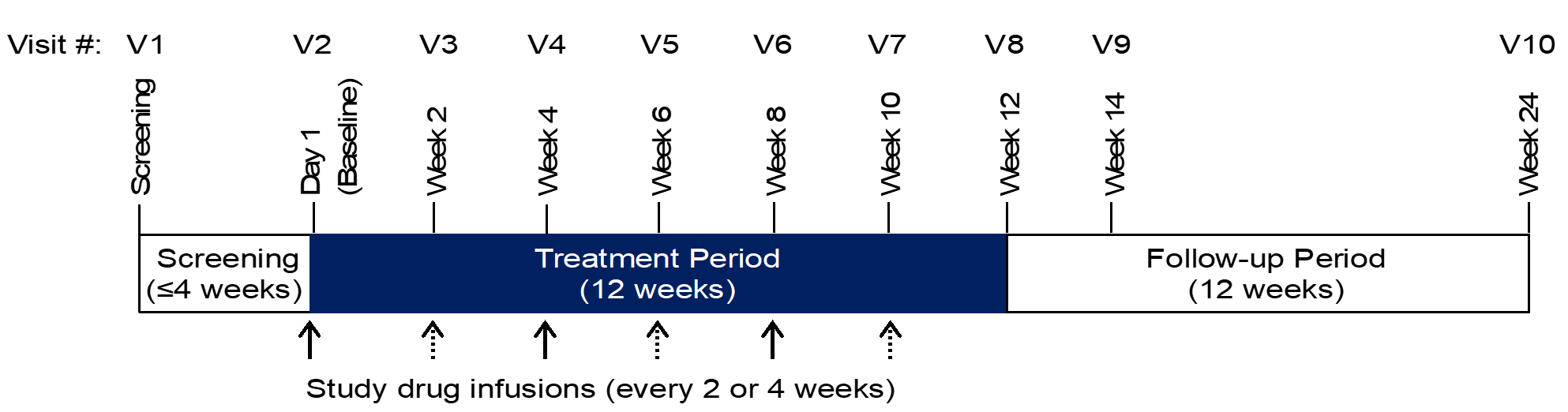
Kurzbeschreibung des gesamten Studiendesigns
|
Beschreibung |
Offene Phase-2-Studie mit ansteigender Mehrfachdosierung zur Bewertung der Wirksamkeit, Sicherheit, Verträglichkeit und Pharmakokinetik von intravenös verabreichtem AMB-05X bei Studienteilnehmer*innen mit TGCT |
|
Stichprobengröße |
Bis zu 48 Studienteilnehmer*innen (bis zu 6 Dosiskohorten) |
|
Region(en) |
USA, Europa, Asien-Pazifik-Raum |
|
Design |
12-wöchige offene Behandlung mit AMB-05X (alle Studienteilnehmer*innen erhalten das aktive Studienmedikament) über 2- bis 4-wöchentliche Infusionen (3 bis 6 Gesamtdosen) |
|
Wesentliche Kriterien für die Teilnahme |
Ø Erwachsene ab 18 Jahren mit bestätigtem TGCT Ø Messbare Erkrankung gemäß RECIST v1.1 nach Beurteilung durch einen zentralen Radiologen |
|
Wesentliche Ergebnisse |
Ø Primäre Wirksamkeit: Gesamtansprechrate (ORR) gemäß RECIST v1.1, bewertet durch einen zentralen Radiologen Ø Sekundäre Endpunkte: Tumor-Volumen-Score, Bewegungsumfang des betroffenen Gelenks, Lebensqualitäts-Skalen, Steifigkeit/Schmerz, Pharmakokinetik, Pharmakodynamik und Sicherheitsparameter |
Die Studie ist derzeit für die Aufnahme von Teilnehmern geöffnet und die Aufnahme wird voraussichtlich bis Juli 2022 fortgesetzt.





